【ELSI】細胞を使うことなく受容体膜タンパク質の人工進化に成功
- ELSI
- 論文
- Space Humanity
―阻害剤感受性を10倍向上させたGタンパク質共役型受容体「アデノシン2A受容体」の新規変異体を同定し、細胞種特異的なシグナル制御を実現―
東京科学大学(Science Tokyo)生命理工学院 生命理工学系の深澤元喜修士課程学生(研究当時)、北尾彰朗教授、同大学 地球生命研究所の松浦友亮教授、福永圭佑特任助教(現:宮崎大学 研究・産学地域連携推進機構 テニュアトラック推進室 准教授)、名古屋大学 大学院工学研究科 松岡佑真博士後期課程学生、清中茂樹教授、千葉大学 大学院理学研究院 村田武士教授らの研究チームは、細胞を用いずに膜タンパク質を実験室内で人工進化させる技術を開発し、リガンド結合能が10倍程度向上したヒト由来アデノシン「A2A受容体(A2AR)」の変異体を同定しました。この変異体を用いることで細胞種特異的なシグナル伝達系の制御が可能です。
細胞外のシグナルを細胞内に伝える役割を担う「Gタンパク質共役型受容体(GPCR: G Protein-Coupled Receptor)」の機能を改変した変異体を、合理的に設計することは、膜タンパク質の柔軟性・不溶化しやすい特性から難しく、多くの試行錯誤を要します。本研究では、無細胞タンパク質合成系とナノディスク技術を組み合わせ、GPCRの1つであるA2ARが機能発現するよう条件を最適化しました。さらに、実験室進化と次世代シーケンサー解析を用いて、変異体集団から特定の阻害剤に対する結合能が向上した変異体を同定しました。変異体は、哺乳動物細胞においてシグナル阻害活性が10倍程度向上しており、この分子機構を原子レベルのシミュレーションで明らかにしました。さらに獲得された変異体の特性を利用し、細胞種特異的にGPCRシグナル伝達を抑制可能であることも示しました。
本研究で開発した手法は、約1012種類規模のGPCRライブラリーから目的の機能を持つ変異体をスクリーニング可能とするものであり、創薬やケモジェネティクス分野における新規GPCR変異体探索の基盤技術となることが期待されます。
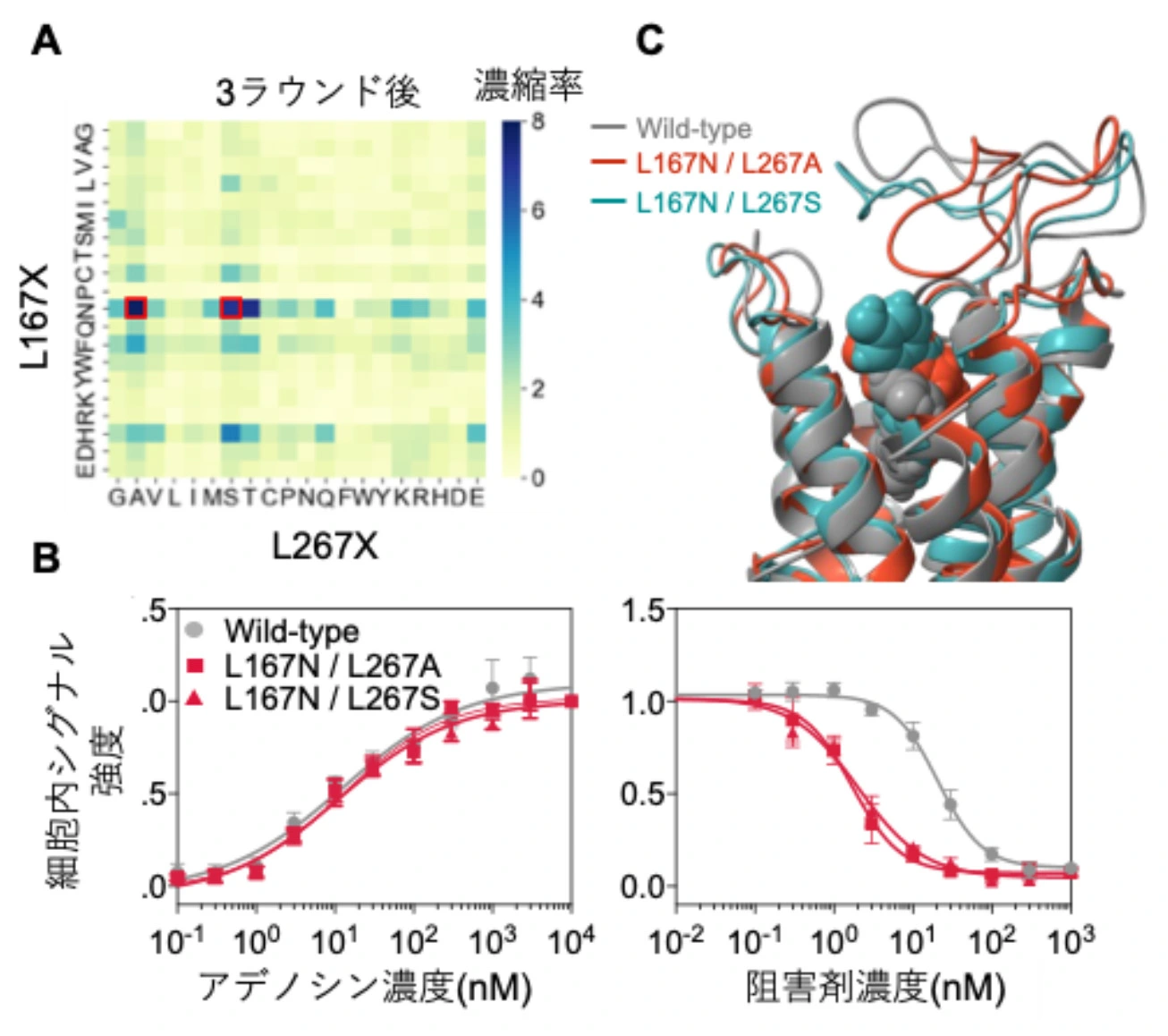
図:人工進化により得られたA2AR変異体
A) NGS解析の結果、400種類の変異体のうち赤で囲った2つが顕著に濃縮されていた
B)取得した2つの変異体は、アデノシンでは野生型と同様に活性化されたが、阻害剤を加えた場合は、野生型よりも10倍低い阻害剤濃度で効果が見られた
C)分子動力学シミュレーションの結果。野生型と変異体は阻害剤と異なる結合様式を持つことが分かった
本成果は、3月6日付(現地時間)の「Journal of the American Chemical Society」誌に掲載されました。
Genki Fukasawa, Yuma Matsuoka, Duy Phuoc Tran, Haruka Nishigaki, Keisuke Fukunaga, Takayoshi Watanabe, Tomohiro Doura, Naohiro Terasaka, Ako Kagawa, Takeshi Murata, Akio Kitao, Shigeki Kiyonaka and Tomoaki Matsuura. In vitro evolution of the adenosine A2A receptor based on an antagonist binding using a ribosome display. Journal of the American Chemical Society. DOI: 10.1021/jacs.6c02372
プレスリリースの全文は、こちらのページをご覧ください。
未来社会創成研究院地球生命研究所(ELSI)については、こちらのページをご覧ください。